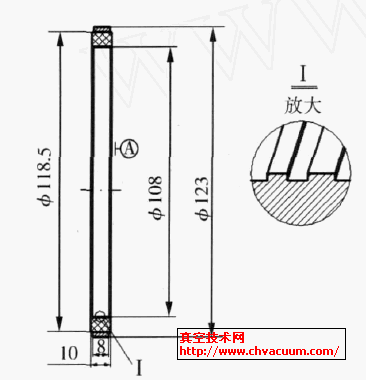
真空热处理对4145H钢H2S腐蚀行为的影响
采用室内浸泡腐蚀试验研究了真空热处理对4145H钢抗H2S腐蚀性能的影响,并分析了其影响机理。利用SEM观察了真空热处理和常压热处理后的4145H钢的组织形貌,利用德国zahner电化学工作站,测试了4145H钢在H2S腐蚀环境中的极化曲线和电化学阻抗谱。结果表明,真空热处理及常压热处理后的组织均为回火托氏体。在H2S溶液中浸泡后的试样的腐蚀类型为局部腐蚀,主要为点蚀。真空热处理降低了试样的表面活性,使其腐蚀电流密度减小。4145H钢在H2S溶液中的阳极溶解动力学符合非催化机制,这是其耐H2S腐蚀性能提高的主要原因。
4145H钢是一种钻铤用钢,钻铤的服役条件十分恶劣,这要求其具有良好的综合力学性能。并且近年来,随着石油资源的日益减少,钻探深度逐渐加深,H2S腐蚀失效已成为引起钻铤断裂的主要原因。目前学界对钢铁抗H2S腐蚀能力做了很多研究,有国外学者指出,热处理工艺对钢铁抗H2S腐蚀能力是有影响的,其中铁素体能力最强,而马氏体能力最弱。前人亦对钻铤用钢各项性能做了相应的研究,但是目前针对钻铤用钢抗硫化氢腐蚀能力的研究少见报道。故本文基于真空热处理和常压热处理的对比,研究了真空热处理对4145H钻铤钢在H2S腐蚀环境中腐蚀行为的影响。
1、实验
1.1、实验材料
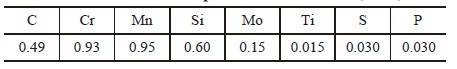
实验材料为4145H钻铤钢,化学成分见表1。实验钢经电弧炉冶炼,铸造成型,并按如下工艺锻造:1200℃保温2h,1150℃锻造,终锻温度950℃。锻造后试样加工成50mm×60mm×120mm的方形试样。
表1 实验钢化学成分(质量分数,%)
1.2、测试溶液
实验中所用溶液为0.1mol/L的饱和硫化氢溶液,其中H2S气体通过FeS与稀硫酸反应制取,并用醋酸调节饱和硫化氢溶液的pH值,最终使实验溶液的pH=2。
1.3、实验方法
实验钢按照表2中工艺进行热处理,真空热处理的真空度为2.5×10-2Pa。热处理后使用线切割机床把试样切割成10mm×10mm×4mm的电化学试样。
表2 实验钢热处理工艺

采用室内浸泡实验模拟石油开采过程中钻铤长期处于硫化氢环境中的腐蚀情况。实验总时间为480h,取样周期分别为72、196、288、360和480h。电化学测试使用德国zahner电化学工作站,测试极化曲线及电化学阻抗。极化曲线扫描范围-0.25~0.5V,扫描速度0.5mV/s。电化学阻抗测试范围0.1~1mHz。
2、结果与讨论
2.1、组织形貌
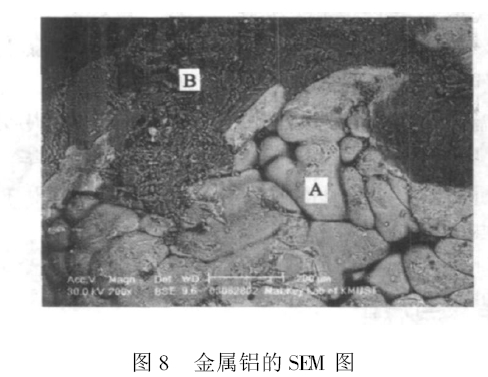
图1是经过热处理后试样1#、2#的组织形貌照片。图中呈条片状的组织是回火后未消除的片条状马氏体的特征,这是典型的回火托氏体。回火托氏体是马氏体中温回火的产物,由于回火温度没能达到马氏体再结晶温度,经过回火后马氏体的片条状特征没有消失。此类组织称为回火托氏体组织。本实验中的实验材料含有一定量的合金元素,因此,提高了马氏体晶粒的再结晶温度,虽然经过600℃以上的回火处理,依然得到了回火托氏体组织。但这种组织在实际生产中有时也被称为回火索氏体。

图1 热处理后组织形貌
2.2、极化曲线
极化曲线是表征电流密度与电极电位关系的曲线。其测试结果表明,在实验周期内,无论试样1#还是试样2#,极化过程的控制步骤均是钢铁表面的活性溶解。并且有研究指出,金属在强酸性溶液中的腐蚀以表面活性溶解为主。从图2中可看出,在实验周期内,试样的腐蚀电流密度随时间的延长而不断增大,但试样2#的腐蚀电流密度明显小于试样1#,根据法拉第定律,其腐蚀速率也同样小于试样1#。应用弱极化区四点法计算腐蚀电流密度,并对计算结果进行二次函数拟合,拟合曲线如图3所示,试样1#的腐蚀电流密度变化规律服从函数y=-6.51+0.01x-8.36×10-6 x2,其符合度为93.7%。试样2#的腐蚀电流密度变化规律服从函数y=-6.31+0.006x-3.58×10-6 x2,其符合度为98.1%。同时,对阳极tafel斜率进行计算,得到试样1#的βa1=14.29mV,试样2#的βa2=24.7mV。
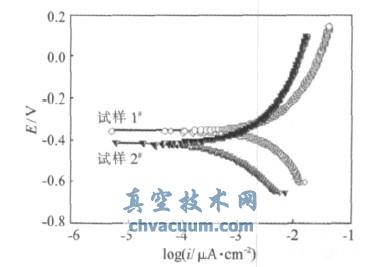
图2 腐蚀360h后测试试样极化曲线
2.3、电化学阻抗谱
图4是腐蚀进行288、360h后的电化学阻抗谱能奎斯特图。直观的,可以以容抗弧曲率半径的大小来衡量被测试样耐蚀性的好坏。从图4中可以看出,试样2#的容抗弧曲率半径明显大于试样1#的容抗弧曲率半径。因此,试样2#的阻抗要大于试样1#,这与前文腐蚀电流密度的结果是相符合的。
同样,电化学阻抗复平面图中高频区和低频的形状也代表了腐蚀过程中不同现象的出现。从图4中可以看出,高频区出现了类似电感的波动,目前学界对这种现象还没有定论,有学者解释为电感的出现,也有学者却认为是测试体系波动造成的。但对于低频区来说,上图试样1#出现了明显的感抗弧,这表明试样表面开始出现点蚀,此时点蚀处于诱导期。并且随着时间的推移,试样1#的感抗弧有加大的倾向,这说明点蚀不断发生并发展。而试样2#虽然有形成感抗弧的趋势,但在低频区并没有出现如试样1#那样明显的现象。这说明试样2#表面的点蚀相对少且浅,在实验周期内点蚀的发展没有试样1#严重。

图3 腐蚀电流密度曲线
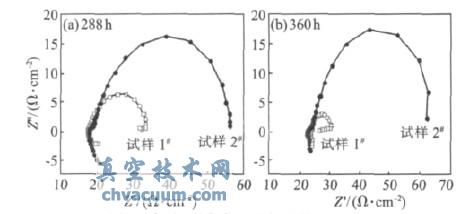
图4 腐蚀不同时间后电化学阻抗图
对于点蚀的生成,有学者认为在某些条件下,酸中钢铁也可以生成点蚀;亦有学者指出Cl-浓度也是引起点蚀的重要原因。本实验中点蚀的形成可能与夹杂物、晶体缺陷或pH值的综合作用有关。
2.4、机理分析
目前,学界对于钢铁在酸溶液中的阳极溶解机理的分析主要集中在非催化机构及催化机构上。催化机制与非催化机制的主要区别在于钢的表面活性强弱,也就是位错等缺陷在钢的表面出现的密度大小。如果钢的表面活性弱、位错密度小,则符合非催化机制;相反的则符合催化机制。
对于非催化机构来说,学界普遍认为铁的活性溶解符合如下反应机构:
Fe+H2O圳Fe(H2O)ad(1)
Fe(H2O)ad→FeOH++e(2)
FeOH++H+圳Fe2++H2O(3)
此反应机构中式(1)与式(3)均是以极快的速度完成,而式(2)的反应速度要慢很多,则对于上述反应机构来说,式(2)是其控制步骤。那么整个铁的活性溶解的腐蚀电流也主要与式(2)的反应速度有关。根据能斯特方程、法拉第定律以及反应速率常数k值的计算公式推导出阳极腐蚀电流密度表达式:
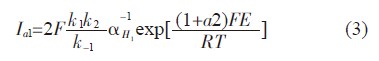
式中:Ia为阳极腐蚀电流密度;F为法拉第常数;αH为氢离子活度;k1为式(1)顺反应速率常数;k-1为式(1)逆反应速率常数;k2为式(2)顺反应速率常数;E为试样自腐蚀电位;R为热力学常数;T为开氏温度;a为对称系数。
根据上式,我们可以很容易地看出钢铁在非催化机构下的阳极溶解反应为1级反应,对于钢铁在酸溶液中,很多实验表明其对称系数a≈0.5,那么本文则取a=0.5。另外根据tafel公式,也可以很容易的计算出阳极tafel斜率βa=17mv。对于催化机构来说,学界并没有形成统一的认识。曹楚南认为此种情况应符合如下反应机构:
Fe+H2O圳Fe(H2O)ad(5)
Fe(H2O)ad圳Fe(OH-)+H+(6)
Fe(OH-)圳(FeOH)ad+e(7)
2(FeOH)ad→FeOH++Fe(OH-)ad(8)
FeOH++H圳Fe2++H2O(9)
对于此反应机构,曹楚南认为式(8)是其控制步骤。同样对此进行推导,得出催化机构下活性溶解腐蚀电流方程如下:
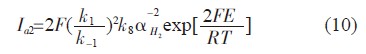
对此方程做如上文处理,计算出催化机构下的阳极tafel斜率βa=12.4mV。
根据前文所述,试样1#的βa=14.3mV,试样2#的βa=24.7mV。可以看出试样1#的β值与上文对催化机制的计算结果βa=12mV相近,因此,试样1#的阳极溶解机理是符合催化机制的。而试样2#的β值与非催化机制相近,因此试样2#符合非催化机制。事实上,真空热处理有利于钢中气体的排除。并且由于真空中对试样的加热没有常压环境中复杂,试样表面没有氧化,使得试样内外受热更均匀,减少了畸变的产生,也使真空热处理后试样符合非催化机制。
3、结论
(1)本实验条件下,4145H钢在湿H2S环境中的腐蚀主要以点蚀为主。
(2)真空热处理后试样的腐蚀电流密度在实验周期内明显小于没有经过真空热处理的试样,经拟合真空热处理后的试样腐蚀电流密度服从函数y=-6.51+0.01x-8.36×10-6 x2。常压处理的试样腐蚀电流密度服从函数y=-6.31+0.006x-3.58×10-6 x2。
(3)真空热处理减少了4145H钢畸变的产生,使其阳极溶解的过程符合非催化机制,这是真空热处理后4145H钢腐蚀电流密度降低的主要原因。