真空碳热还原分解硫酸钙热力学分析及实验探究
采用“物质吉布斯自由能法”讨论在常压和体系压强为50 Pa 条件下,硫酸钙碳热还原分解的热力学条件并进行了实验探究。计算得出: 在常压条件下,在500 ~ 800 K 时,硫酸钙与碳反应生成CaS,当温度升至1400 K 以上时,CaS 与CaSO4发生反应生成CaO; 当系统压强为50 Pa 时,第一步反应温度为400 ~ 600 K,第二步则降至1100 K 以下。实验结论: 反应明显分两步发生,第一阶段在400 ~ 600 K,第二阶段反应起始于950 ~ 1000 K,最终固体产物主要为CaO,含有少量CaS。实验验证了理论计算的正确性,为硫酸钙真空碳热分解提供热力学理论依据和实验基础。
中国有着丰富的石膏资源,仅天然石膏储量为576 亿吨,此外,每年还产生大量工业副产石膏,如火力发电站中脱硫系统产生的脱硫石膏,二氧化钛生产中产生的钛石膏,磷肥、磷酸生产的副产品磷石膏,氢氟酸生产中产生的氟石膏,柠檬酸生产中产生的柠檬酸石膏等,其中仅磷石膏每年的排放量达两亿多吨,逐渐成为一种数量巨大、环境污染严重的固体废弃物,其大量堆放不仅占用大量土地资源,污染空气、水源及土壤等,同时造成了大量硫资源的浪费。
工业石膏的处理及综合利用成为国内外学者密切关注和研究的课题,目前对于磷石膏制酸联产水泥作了深入研究,并一直被认为是最合理并能从根本解决工业石膏问题的有效方法,这不但为硫酸工业、水泥工业提供廉价原料,还能大幅度降低二氧化碳排放量。但在此过程中,真空技术网(http://www.chvacuum.com/)认为存在耗能高,成本高等缺点,硫酸钙直接热解也存在反应温度高,分解时间长等问题。因此,本文提出对硫酸钙进行真空碳热还原分解研究,探究硫酸钙在真空条件下碳热还原分解热力学条件,并实验进行验证,以期达到降低硫酸钙分解能耗,合理利用工业废石膏的目的。
1、实验
1.1、实验原料与设备
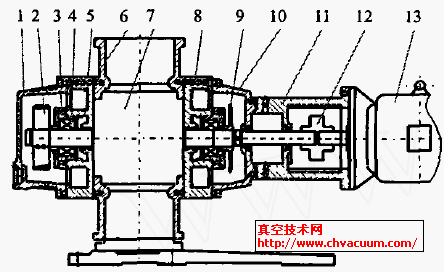
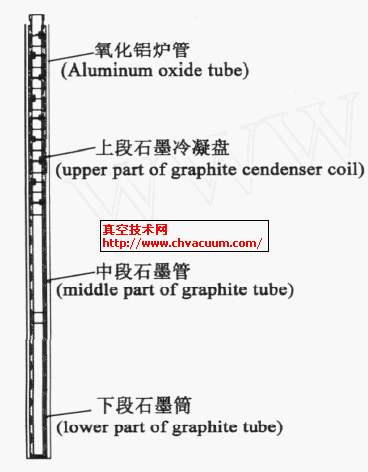
实验原料为分析纯硫酸钙,石墨粉;实验设备为使用实验室自行设计的小型立式真空炉。
1.2、实验过程
将硫酸钙球磨并筛分- 140 目。每次实验根据C /S 摩尔比,称取一定质量的CaSO4粉末和石墨粉,混合均匀,在7 ~ 9 MPa 的压力下压制成块( Φ20mm × 25 mm) ,置于石墨坩埚中,并放入真空炉中,密封真空炉。打开循环冷却水,抽真空至极限真空度( 20~ 30 Pa) ,然后以10 ~ 15℃ /min 的升温速率升至一定温度后恒温,恒温保温一定时间后停止加热,继续抽真空直到温度降至100℃ 以下,停泵,关闭冷却水,开炉取样。
1.3、分析检测
采用日本理学公司Rigaku X 射线自动衍射( XRD) ( TTRIII) 对反应残渣进行物相分析,使用CuKα,扫描区间为10° ~ 90°。
2、理论计算
2.1、常压条件下硫酸钙碳热还原分解的热力学分析
在CaSO4碳热还原分解过程中,CaSO4与C 之间的反应复杂多样,具体反应如表1。
表1 CaSO4与C 之间可能发生的反应

3、结论
(1) 理论计算结论: 硫酸钙碳热还原分解分两步发生,在500 ~ 800 K 分解生成CaS,1400 K 以上CaS 与未反应CaSO4发生固-固反应,生成CaO; 在真空条件下,第一步反应将在400 ~ 600 K 之间完成,第二步反应降至1080 K 发生。
(2) 实验结论: 采用真空碳热还原分解CaSO4实验表明,在真空条件下,第一阶段反应集中发生在400 ~ 600 K,在800 ~ 1000 K 之间体系没有发生变化,1000 K 以上发生第二阶段反应,最终主要产物为CaO。
(3) 通过不同反应温度、不同配碳量对比试验表明: 当S /C = 2:1,反应温度为1373 K 时,硫酸钙分解完全,且CaS 转化率高。