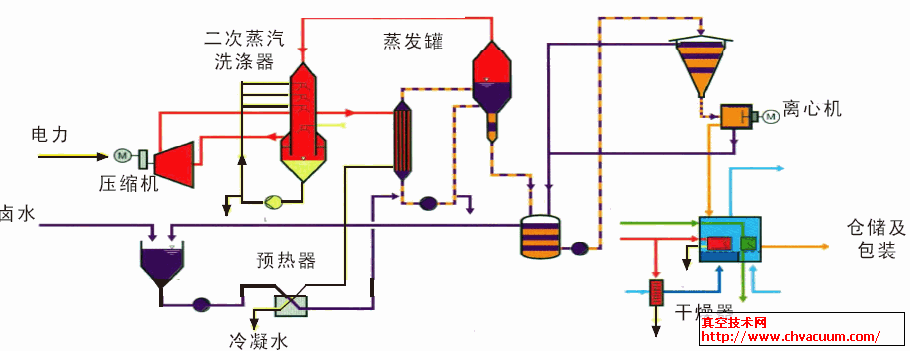
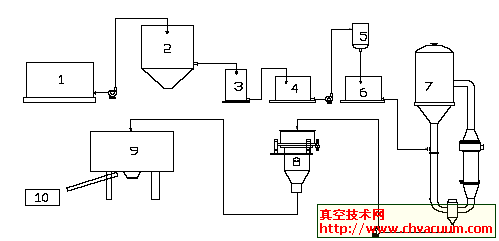
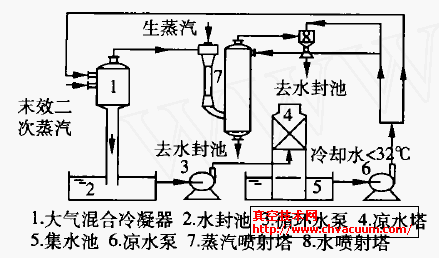
两种硫酸根含量测定方法的比较
为了更快更准确地测定出卤水中硫酸根离子的含量,参照国家标准方法,我们对两种硫酸根含量的测定方法--分光光度法和容量滴定法进行了比较。
1、前言
湖北沙隆达股份有限公司盐矿是由企业自筹资金、自主开发的盐矿,由于地质结构原因,硫酸根含量一直较高。为了了解采层矿物质构成,同时为下一步硫酸根处理工序提供依据, 我们必须对开采出的卤水中的硫酸根含量进行快速准确的分析。参照国家标准方法, 我们对分光光度法和容量滴定法进行了比较,以期找到一种同时具有简便、快捷、准确等特性的实验方法。
2、原理
2.1、分光光度法
在酸性介质中,一定浓度SO42-与Ba2+生成Ba-SO4沉淀。加入酸-盐-甘油试剂可以帮助形成物理性质均匀的细粒并阻止沉淀的沉降而呈现悬浮物状态,在420nm处测其吸光度。在一定浓度范围内,服从郎白-比尔定律,即A=£bc
SO4 2- +Ba2+→ BaSO4
2.2、容量滴定法
在酸性介质中, 氯化钡与样品中的硫酸根生成难溶的硫酸钡沉淀,过剩的钡离子在pH=10 的介质中以铬黑T 作指示剂, 用EDTA 标准溶液滴定,间接测定硫酸根含量。
3、仪器
3.1、722 或721 型分光光度计(配比色皿一套);
3.2、50mL具塞比色管一套;
3.3、一般实验室常用玻璃仪器。
4、试剂及制备方法
4.1.1、特备试剂: 将50mL甘油,30mL浓盐酸,300mL蒸馏水,100mL95%乙醇,75克氯化钠混匀。
4.1.2、0.25g/mL氯化钡溶液: 取25克氯化钡溶于100mL蒸馏水中。
4.1.3、硫酸根标准贮备溶液(10mg/mL):准确称取7.3930g(称准至0.0001g)已烘干的基准硫酸钠(G、R)溶于100mL 水中,全量转入500mL 容量瓶中,加水定容,摇匀。
4.1.4、硫酸根标准使用溶液(1mg/mL): 准确移取10.00mL 硫酸钠标准贮备溶液于100mL 容量瓶中,加水定容,摇匀。
4.2.1、20g/L 盐酸羟胺溶液:称取10 克盐酸羟胺固体,用蒸馏水溶解并稀释至500 毫升。
4.2.2、30%三乙醇胺溶液: 量取150mL 三乙醇胺,用蒸馏水溶解并稀释至500mL,贮存于棕色瓶中。
4.2.3、5g/L 铬黑T: 称取0.5g 铬黑T 和5g 盐酸羟胺, 溶于25mL 无水乙醇, 用三乙醇胺稀释至100mL,贮存于棕色瓶中。
4.2.4、50g/L 乙二胺四乙酸二钠镁:称取50 克乙二胺四乙酸二钠镁(四水盐),溶解于无二氧化碳纯水中,稀释至1000 毫升。
4.2.5、0.05mol/L 氯化钡标准溶液。
5、分析步骤
5.1、分光光度法
5.1.1、标准曲线的绘制: 精确吸取硫酸根标准溶液1、2、3、4、5mL 于5 个150mL 烧杯中分别加入100mL 蒸馏水、5mL特备试剂,在搅拌器上搅匀。同时加入1.0mL0.25g/mL 氯化钡溶液, 匀速搅拌1分钟,将浑浊液倒入1 厘米比色皿中,静置4 分钟,在420nm 处,以蒸馏水作空白,分别测其吸光度。以吸光度为横坐标, 以吸取硫酸根标准溶液的毫升数为纵坐标绘制标准曲线。
5.1.2、样品的测定: 吸取卤水10.0mL 于100mL 容量瓶中,用蒸馏水稀释至刻度,摇匀静置。从中精确吸取2.0mL 卤水稀释溶液于150mL 烧杯中。加入98mL 蒸馏水及5mL 特备试剂,在搅拌器上搅匀,同时加入1mL 氯化钡溶液,匀速搅拌1 分钟。将浑浊液倒入1 厘米比色皿中,静置4 分钟,在波长420nm处,以蒸馏水作空白,测其吸光度。
5.1.3、计算
SO42- (g/L)=E1×V1/E2×V
式中:E1———样品的吸光度;
E2———硫酸根标准溶液的吸光度;
V1———吸取硫酸根溶液的mL 数;
V———吸取卤水样品的mL 数。
5.2、容量滴定法
5.2.1、准确吸取5.00mL试样, 置于250mL 锥形瓶中,加盐酸2 滴即1mL(视样品碱性强弱而定)酸化,从滴定管中加入氯化钡标准溶液10~30mL(视样品中硫酸根离子浓度而估加),注意边摇边加,以减少沉淀的吸附,记录加入的体积数V1(mL)。用1~2mL蒸馏水冲洗锥形瓶内壁,加热微沸2 分钟,并冷至室温,加入10mLMg-EDTA 溶液、10mL 无水乙醇、2mL盐酸羟胺、3mL 三乙醇胺、10mL 缓冲溶液、3~5 滴铬黑T 指示剂, 注意每加入一种试剂均需摇匀。用EDTA 标准溶液滴定至溶液由紫红色变为纯兰色为终点。记录消耗EDTA 标准溶液的体积V2(mL)。
5.2.2、准确吸取5.00mL 试样, 置于250mL 锥形瓶中,加入20mL 蒸馏水,加盐酸溶液2 滴~1mL 酸化,加入2mL 盐酸羟胺、3mL 三乙醇胺、10mL 缓冲溶液、3~5 滴铬黑T 指示剂,注意每加入一种试剂均需摇匀。用EDTA 标准溶液滴定至溶液由紫红色变为纯兰色为终点。记录消耗EDTA 标准溶液的体积V0(mL)。
5.2.3、计算
SO42-(g/L)=[C1V1-C2(V2-V0)]×96.06/5
式中: C1———氯化钡标准溶液的浓度,mol/L;
V1———氯化钡标准溶液的体积,mL;
C2———EDTA 标准溶液的浓度,mol/L;
V2———测定样品时消耗EDTA 溶液的体积,mL;
V0———测钙镁总量时,5.00 试样所消耗EDTA 溶液的体积,mL;
96.06———1mol 硫酸根的质量,g。
6、对比实验
取同一标准溶液用上述两种分析方法进行SO42-分析,从以下两个方面进行对比
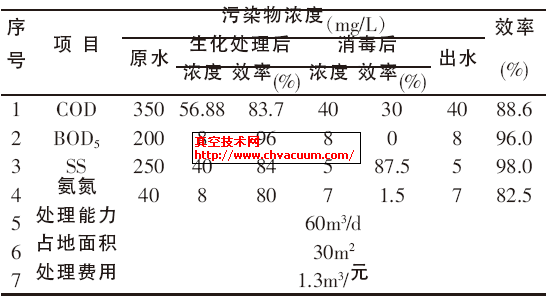
6.1、准确度对比:取8.00g/L SO42-标准溶液,按照以上两种分析方法进行6 组测定。数据见下表。
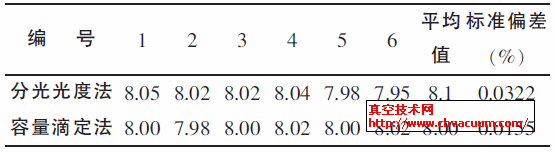
6.2、分析时间对比:以上6 组实验,分光光度法平均用时8.2分钟,容量滴定法用时18.0 分钟。
7、方法评价
7.1、容量滴定法与分光光度法相较准确度与精密度更高, 适用于对准确度要求更高的样品的实验检测。
7.2、分光光度法对仪器要求更高,其特点是更为快捷,适用于大批量样品的实验检测。